Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
中島 隼人; 清水 三郎; 小貫 薫; 池添 康正; 佐藤 章一
日本化学会誌, 8, p.1257 - 1261, 1984/00
ニッケル、ヨウ素、硫黄系熱化学水素製造プロセスに含まれる反応であるNil の熱分解反応について、熱天秤を用い速度論的な検討を行った。反応温度775K-869Kヨウ素分圧0-960PaにおけるNil
の熱分解反応について、熱天秤を用い速度論的な検討を行った。反応温度775K-869Kヨウ素分圧0-960PaにおけるNil ペレットの熱分解反応は表面から起り、反応初期より中期にかけて界面反応過程が律速であると考えられる。見かけの分解反応速度は、一定反応温度で一定値である正反応の速度と、ヨウ素分圧に比例する逆反応の速度の和で表わされる。この正反応の速度は、ヨウ素分圧0のときの分解反応速度であり、その温度でのヨウ化ニッケルの平衝解離圧に比例する。見かけの分解反応の活性化エネルギーは147KJ・mol
ペレットの熱分解反応は表面から起り、反応初期より中期にかけて界面反応過程が律速であると考えられる。見かけの分解反応速度は、一定反応温度で一定値である正反応の速度と、ヨウ素分圧に比例する逆反応の速度の和で表わされる。この正反応の速度は、ヨウ素分圧0のときの分解反応速度であり、その温度でのヨウ化ニッケルの平衝解離圧に比例する。見かけの分解反応の活性化エネルギーは147KJ・mol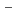
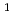 と求められ平衝圧から算出した反応熱に極く近い。
と求められ平衝圧から算出した反応熱に極く近い。
清水 三郎; 佐藤 章一; 中島 隼人; 小貫 薫
電気化学および工業物理化学, 50(11), p.898 - 903, 1982/00
ニッケル塩-エタノール2成分系と混合ニッケル塩-水3成分系の溶解度を測定した。その結果、NISプロセスに不可欠なヨウ化ニッケル(II)と硫酸ニッケル(II)の分離法として、次の2方法が有効であることを見出した。第1の方法は、無水エタノールのかわりに5~10wt%の含水エタノールを溶剤として乾燥混合塩からヨウ化物のみを抽出する方法である。第2に方法は、濃厚な混合水溶液から硫酸ニッケル(II)含水塩が選択的に晶析することを利用する分離法である。25 Cでの、ヨウ化ニッケル(II)540gを含む100g溶液中の、硫酸ニッケル(II)7水塩共存下における硫酸ニッケル(II)溶解度は0.5gである。晶析分離法を採用することにより、水素1モル当りの熱所要量は2538kJから1736kJへ減少した。
Cでの、ヨウ化ニッケル(II)540gを含む100g溶液中の、硫酸ニッケル(II)7水塩共存下における硫酸ニッケル(II)溶解度は0.5gである。晶析分離法を採用することにより、水素1モル当りの熱所要量は2538kJから1736kJへ減少した。
清水 三郎; 小貫 薫; 中島 隼人; 池添 康正; 佐藤 章一
電気化学および工業物理化学, 50(11), p.904 - 908, 1982/00
NISプロセスで水素を製造するために必要な熱量1746kJ/molH のうちの42%をヨウ化ニッケル(II)含水塩系の乾燥のために用いる。この塩の乾燥のための基本データである平衡水蒸気圧測定を行い、次のことを明らかにした。(1)平衡水蒸気圧は二つの蒸気圧式であらわされる:logP(atm)=8.23-3.15
のうちの42%をヨウ化ニッケル(II)含水塩系の乾燥のために用いる。この塩の乾燥のための基本データである平衡水蒸気圧測定を行い、次のことを明らかにした。(1)平衡水蒸気圧は二つの蒸気圧式であらわされる:logP(atm)=8.23-3.15 10
10 /T(22.3~60.3
/T(22.3~60.3 C)、logP=6.34-2.52
C)、logP=6.34-2.52 10
10 /T(60.3~134.3
/T(60.3~134.3 C)。(2)ヨウ化ニッケル(II)水和物では低次の安定な水和物は存在しない。この点は、低昇温速度熱重量分析で確かめられた。(3)含水塩中の水は60.3
C)。(2)ヨウ化ニッケル(II)水和物では低次の安定な水和物は存在しない。この点は、低昇温速度熱重量分析で確かめられた。(3)含水塩中の水は60.3 C以上では結晶水から液体状態の水へ転移すると考えられる。(4)蒸気圧式より本含水塩の乾燥は136
C以上では結晶水から液体状態の水へ転移すると考えられる。(4)蒸気圧式より本含水塩の乾燥は136 C、蒸気圧1.5atmの条件下で実施でき、また蒸発潜熱は蒸気圧縮法で回収し得る。
C、蒸気圧1.5atmの条件下で実施でき、また蒸発潜熱は蒸気圧縮法で回収し得る。